За гранью привычного: исследование эффективности прибора TrueScreen в сравнении с ПАП-тестом при обнаружении рака шейки матки.
Цели исследования: Целью исследования является рассмотрение возможности использования оптоэлектронного прибора (TruScreen™; TS) для скрининга в режиме реального времени в качестве альтернативы или дополнения к ПАП-тесту (жидкостной цитологии (LBC)) для скрининга рака шейки матки.
Метод: Мы провели проспективное наблюдательное исследование, в котором приняли участие женщины, регулярно наблюдавшиеся в гинекологических клиниках в период сбора данных. Когда исследование было инициировано, все женщины, отвечающие критериям отбора, периодически проходили обследование с помощью TS и LBC. Женщинам, у которых были выявлены отклонения, необходимо было пройти кольпоскопию и биопсию шейки матки в течение одного месяца с момента получения неудовлетворительных результатов скрининга.
Результаты: Итого 507 женщин соответствовали критериям отбора и приняли участие в исследовании, из них 30 женщин (5,9%) с неудовлетворительными результатами после проверки на приборе TS прошли процедуру кольпоскопии. У 13 женщин (43,3 %) были обнаружены поражения низкой степени, и только у одной (3,3 %) были выявлены поражения высокой степени. Что касается результатов биопсии, у трех женщин была цервикальная интраэпителиальная неоплазия (CIN) I, у двух женщин - CIN II+, и у одной - железистая гиперплазия. Чувствительность TS составила 83,3% (95% ДИ: 35,9-99,6%) и специфичность 95% (95% ДИ: 92,7-96,8%) для выявления патологически диагностированной цервикальной неоплазии, по сравнению с 66,7% (95%: ДИ 22,3-95,7%) и 98,2% (95% ДИ 96,6%-99,2%) для ПАП-теста. Разница между обоими скрининговыми инструментами не была статистически значимой (p=0,91). Чувствительность (100%, 95% CI 15,6-100%) и специфичность (95,6%, 95% CI 93,4-97,2%) TS и ПАП-теста для поражений CIN II+ были достоверно высокими.
Заключение: TS представляет собой надежный и практичный инструмент скрининга цервикальной неоплазии, не требующий взятия образцов шейки матки, наличия лабораторного оборудования и обученного персонала. Наше исследование показало, что данный прибор обеспечивает точные результаты скрининга в режиме реального времени, что делает его пригодным для обследования женщин, подверженных риску развития рака шейки матки.
Введение
Во всем мире карцинома шейки матки занимает четвертое место по частоте среди онкологических заболеваний и является одной из основных причин смертности от рака у женщин [1]. По данным Глобальной статистики заболеваемости раком (GLOBOCAN 2020), в 2020 году рак шейки матки был диагностирован примерно у 604 000 женщин, а смертность составила 342 000 женщин [2]. Показатели заболеваемости и смертности от рака шейки матки были значительно выше (около 85%) в странах с низким и средним уровнем дохода, в то время как в развитых странах они составили всего 3,6% [3]. Такой рост заболеваемости и смертности в значительной степени коррелирует с отсутствием программ скрининга рака шейки матки [4, 5].
Инфицирование вирусом папилломы человека (ВПЧ) является одним из основных факторов риска развития рака шейки матки, поскольку инфекция может привести к цервикальной интраэпителиальной неоплазии (CIN) [6]. Тем не менее, для прогрессирования поражения от CIN II+ до инвазивного рака требуется около 5-10 лет [7]. Поэтому рак шейки матки считается предотвратимой злокачественной опухолью, и существуют большие возможности для раннего выявления предраковых поражений с помощью скрининговых методов [8, 9].
В связи с этим Всемирная организация здравоохранения (ВОЗ) поставила цель ликвидировать рак шейки матки к 2030 году с помощью комплексного подхода, включающего программы профилактики, ранней диагностики, эффективного скрининга и лечения [10]. Профилактика рака шейки матки имеет решающее значение для снижения заболеваемости и достижения целей устойчивого развития в области здравоохранения [11]. Более того, существует множество вакцин для защиты от распространенных типов ВПЧ, вызывающих рак [12].
Кроме того, для снижения заболеваемости и смертности от рака шейки матки крайне важна ранняя диагностика, однако во многих странах, в том числе в Саудовской Аравии, отсутствуют национальные программы скрининга. Криотерапия или петлевая электрохирургическая эксцизионная процедура (LEEP) являются эффективными методами абляции для женщин, у которых были выявлены патологические поражения. Чтобы предотвратить развитие рака или вылечить его на ранней стадии, ВОЗ рекомендует следующие методы скрининга: ВПЧ, цитология и визуальная инспекция шейки матки после обработки уксусной кислотой (VIA) для женщин, у которых просматривается зона трансформации [5].
За последние несколько десятилетий возросла важность национальных программ скрининга для выявления ранних стадий рака шейки матки. ПАП-тест, т.е. традиционная цитология, является наиболее часто используемым тестом, однако он имеет ограничения в отношении чувствительности и специфичности. Частота ложноотрицательных результатов достигает 53 %, что связано с субъективными ошибками при подготовке и оценке мазка [5, 13]. Кроме того, результаты цитологии не могут быть получены оперативно, что увеличивает риск прекращения женщинами последующего наблюдения. Во многих странах, в том числе в Саудовской Аравии, для получения результатов цитологического скрининга в течение одной-двух недель требуется два визита.
Кольпоскопическая оценка после аномальных цитологических изменений является диагностическим инструментом, точность которого выше, чем у традиционной цитологии, а общая чувствительность и специфичность оцениваются в 80% и 92% соответственно [14, 15]. Кольпоскопия считается экономически эффективной диагностической концепцией, особенно в условиях ограниченности ресурсов. Однако для точной оценки результатов требуется опыт визуальных наблюдений и высокая квалификация медицинских работников [16-18]. С развитием научных технологий появился новый оптоэлектронный прибор, сканирующий в режиме реального времени, под названием TruScreen (TS). Его использование подразумевается в рамках экспертного системного подхода на основе искусственного интеллекта. Он обладает существенными преимуществами, являясь высоко объективным, неинвазивным, простым и самоконтролируемым инструментом с получением результатов в режиме реального времени и минимальными затратами ресурсов [5, 19]. Несколько исследований подтвердили клиническую валидацию прибора TS [5, 20-22], а в многоцентровом исследовании изучалась эффективность скрининга с помощью комбинации TS и ПАП-теста [23]. Оно показало, что данная комбинация повышает чувствительность диагностики CIN III+ с 69 до 93 % [23].
Несмотря на реализацию нескольких скрининговых программ, заболеваемость раком шейки матки в регионе Ближнего Востока остается значительной. Несмотря на наличие сообщений об использовании TS для скрининга рака шейки матки за последние несколько лет, в регионе Ближнего Востока количество таких упоминаний является минимальным. Поэтому целью данного исследования было определить, можно ли использовать оптико-электронный прибор для скрининга в режиме реального времени (TruScreen™) в качестве альтернативы или дополнения к ПАП-тесту (жидкостной цитологии) для скрининга рака шейки матки.
Пациенты и методы
Отчет о данном исследовании был подготовлен в соответствии с положениями Стандартов отчетности об исследованиях диагностической точности (STARD) [24]. Протокол исследования был одобрен Институциональным наблюдательным советом (IRB) (Ref No. Dr. Sulaiman Al-Habib Medical Group - RC20.08.91- Aug 2020). Все пациенты должны были подписать информированное согласие перед участием в исследовании.
План и предметы исследования
Мы провели проспективное наблюдательное многоцентровое исследование, в котором участвовали женщины, находившиеся под плановым наблюдением в гинекологических клиниках и больницах Тахассуси Медицинской группы Аль-Хабиб, Арраян, Олайя, Эр-Рияд, Саудовская Аравия, с января 2021 по январь 2022 года. В исследовании приняли участие пятьсот девяносто одна женщина в возрасте 23-65 лет, каждая из которых последовательно посещала амбулаторную гинекологическую клинику во время сбора данных. В исследовании могли принять участие все женщины репродуктивного возраста, которые посещали амбулаторные гинекологические клиники в течение исследуемого периода. Критерии участия включали согласие на участие в исследовании и подписание информированного согласия, отсутствие в анамнезе гистерэктомии, менструации, беременности или послеродового периода. Женщины с подтвержденным диагнозом карциномы или с любой вагинальной инфекцией были исключены из исследования.
После подтверждения участия все женщины, отвечающие критериям отбора, прошли внеплановое обследование с использованием TS и ПАП-теста у гинекологов (прошедших соответствующую подготовку по TS). Женщины, у которых были обнаружены отклонения, должны были пройти кольпоскопию и биопсию шейки матки в течение одного месяца. Перед обследованием были собраны следующие данные: возраст, этническая принадлежность, стаж курения, акушерский анамнез, наличие промежуточных менструальных кровотечений, наличие вируса иммунодефицита человека (ВИЧ), история ВПЧ или папиллом, прием иммунодепрессантов, метод контрацепции, статус вакцинации против ВПЧ и история предыдущих ПАП-тестов.
Обследование при помощи TruScreen и ПАП-теста
Исследование TS проводилось на аппарате TruScreen Pty Ltd (NZX/ASX: TRU) с участием женщины, находящейся в лиотомическом положении. Прибор производит оценку состояния шейки матки в режиме реального времени после активации одноразового фотоэлектрического датчика на >15 участках эпителия шейки матки.
TruScreen - это прибор, обеспечивающий оптоэлектронный скрининг в режиме реального времени, который позволяет выявлять предраковые и раковые поражения шейки матки путем сравнения оптических и электро-физических характеристик и поведения исследуемой ткани с характеристиками известных типов тканей.
Прибор состоит из ручного зонда, соединенного с беспроводной зарядной подставкой Qi с электромагнитной индукцией. Общая длина прибора от основания до кончика составляет около 37 см (рис. 1-3). Длина части зонда, вводимого во влагалище, составляет 120 мм, а диаметр его кончика - около 5 мм. Наконечник зонда также покрыт оболочкой, в которую встроен одноразовый датчик, что увеличивает диаметр наконечника примерно до 6,5 мм.
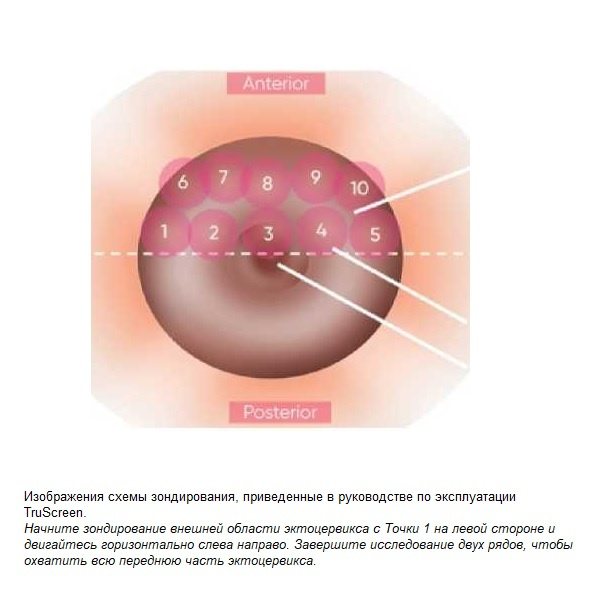
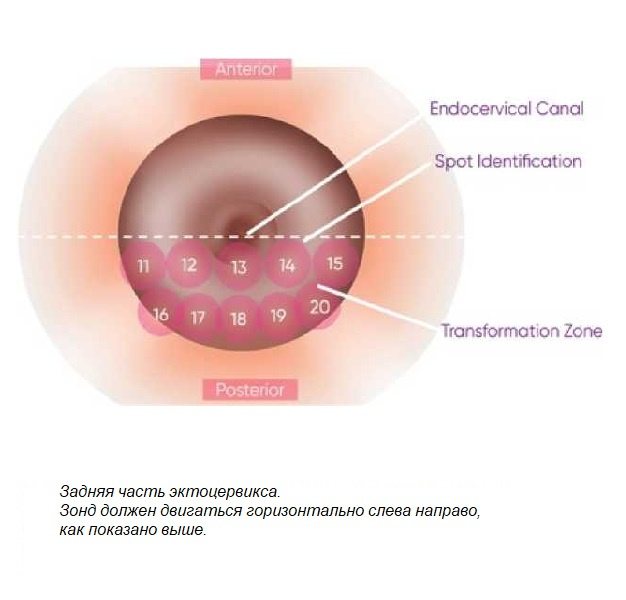
Прибор классифицировал все результаты как нормальные или отличающиеся от нормы. Никто из специалистов не был ознакомлен с результатами предыдущих ПАП-тестов, и исследование проводилось без кольпоскопической визуализации. Аналогичным образом, сотрудники лаборатории не были ознакомлены с результатами TS. ПАП-тест проводился с использованием жидкостной цитологии, а результаты интерпретировались в соответствии с системой Bethesda 2001 года [25]. TS и ПАП-тест проводились во время одних и тех же сеансов.
Кольпоскопия и биопсия
Женщины с неудовлетворительными результатами TS или ПАП-теста направлялись на кольпоскопическое обследование к квалифицированному гинекологу. Из участков, в которых были обнаружены отклонения, бралась биопсия и отправлялась на гистопатологию. Пациенткам, у которых не удалось полностью обследовать плоско-столбчатое соединение, проводилось выскабливание эндоцервикального канала. Ведение пациенток основывалось на двухуровневой системе классификации патологии с делением на поражения низкой степени (CIN I) и рак шейки матки (CIN II+ и CIN III+) [26].
Статистический анализ
Объем выборки был рассчитан для выявления значительной чувствительности, учитывая, что распространенность CIN II+ в лечебно-диагностических центрах колеблется от 5 до 20 %. Исходя из данного показателя распространенности и 95% доверительного интервала (95% ДИ), объем выборки в 600 пациенток был консервативной оценкой для исследования, охватывающего большинство гинекологических аномалий. Среди пациенток, выбранных для оценки клинической эффективности, наблюдается более высокая распространенность аномальных образований по сравнению с общей популяцией, что позволяет оценить чувствительность и частоту ложноотрицательных результатов при оценке работы прибора. Также учитывались случаи прерывания обследования до 20%.
Статистический анализ проводился с помощью программы Stata версии 16.0 (Stata Corp LLC, College Station, TX 77845, США). Данные обобщались с учётом вероятных отклонений и обычных статистических колебаний для получения непрерывных параметров, в то время как для определения категориальных переменных использовались подсчеты и проценты. Эффективность скрининга посредством TS и ПАП-теста рассчитывалась с учётом доверительного интервала 95% (ДИ), чувствительности (количество пациентов с патологическими поражениями, у которых были выявлены неудовлетворительные результаты, деленное на всех пациентов с патологическими поражениями х 100), специфичности (количество пациентов с нормальными результатами, деленное на всех пациентов с нормальной патологией х 100), положительной предсказательной ценности (PPV) (количество пациентов с истинно положительными результатами, деленное на количество пациентов с истинно положительными и ложноположительными результатами х 100), а также отрицательной предсказательной ценности (NPV) (количество пациентов с истинно отрицательными результатами, деленное на общее количество пациентов с отрицательными результатами х 100). Тест хи-квадрат или точный тест Фишера использовался для сравнения эффективности скрининга с помощью TS и ПАП-теста, в зависимости от ситуации. Статистически значимым считалось значение p-value < 5%.
Результаты
В исследовании приняла участие 51 женщина; 84 из них были исключены из исследования. Пятьсот семь женщин соответствовали критериям отбора и приняли участие в исследовании, их средний возраст составил 38,7 ± 8,5 лет (диапазон 23-61). Большинство женщин были арабского происхождения (79,3%), и только (4,7%) из них курили. В целом, 22,5% и 12,6% женщин сообщили о наличии отклоняющихся от нормы вагинальных и посткоитусных кровотечений в анамнезе, соответственно. Семьдесят девять женщин (15,6%) принимали один или несколько методов контрацепции, в основном комбинированные пероральные контрацептивы. Только у одной женщины (0,2%) был обнаружен ВИЧ, а у 16 женщин (3,2%) в анамнезе присутствовал ВПЧ / вагинальные папилломы. Почти 27% женщин сообщили о предыдущих результатах ПАП-теста, и в 18,7% из них присутствовали отклонения от нормы.
Таблица 1: Демографические и исходные характеристики женщин, участвующих в исследовании
Переменные |
Женщины (n =507) |
Возраст (год), вероятные отклонения ± обычные статистические колебания |
38.7 ±8.5 |
Этническая принадлежность, N (%) арабского происхождения |
402 (79.3) |
индийского происхождения |
16 (3.1) |
азиатского происхождения |
57 (11.2) |
африканского происхождения |
2 (0.4) |
кавказского происхождения |
11 (2.2) |
Прочее |
19 (3.7) |
Курение N (%) |
24 (4.7) |
Способность к деторождению, вероятные отклонения ± обычные статистические колебания |
2.7 ±1.9 |
Отклоняющиеся от нормы вагинальные кровотечения, N (%) |
114 (22.5) |
Посткоитальные кровотечения, N (%) |
73 (14.4) |
Контрацепция, N (%) |
79 (15.6) |
Тип контрацепции, N (%) Комбинированные контрацептивы |
42 (8.3) |
IUCD |
30 (5.9) |
IMPLANON /DEPO/pop |
6 (1.2) |
Выявленный ВИЧ, N (%) |
1 (0.2) |
ВПЧ / вагинальные папилломы, N (%) |
16 (3.2) |
Употребление иммунодепрессантов, N (%) |
7 (1.4) |
Вакцинация от ВПЧ, N (%) |
6 (1.2) |
Результаты предыдущего ПАП-теста, N (%) |
136 (26.8) |
Результаты ПАП-теста1, N (%) В пределах нормы |
106 (77.9) |
Отклонения от нормы |
25 (18.7) |
Неудовлетворительные |
1 (0.7) |
Предыдущий тест на ВПЧ, N (%) |
9 (1.8) |
Сокращения: UCD - внутриматочное противозачаточное средство; ВИЧ - вирус иммунодефицита человека; ВПЧ - вирус папилломы человека.
1 n =136
Результаты, полученные с помощью TruScreen, ПАП-теста, кольпоскопии и биопсии
В целом, у 30 женщин (5,9%) отклонения от нормы были обнаружены с помощью прибора TS, а результаты ПАП-теста распределились следующим образом:
- норма (75%)
- атипические клетки плоского эпителия неясного значения (ASCUS) (0,6%)
- плоскоклеточные интраэпителиальные поражения низкой степени (LSIL) (0,8%)
- плоскоклеточные интраэпителиальные поражения высокой степени (HSIL) (0,4%)
- воспалительные/реактивные клетки (21,1%)
- клетки эндометрия (1%) и неудовлетворительные результаты (1,2%).
При сопоставлении результатов TS с результатами ПАП-теста было обнаружено следующее:
у 14 женщин с нормальными результатами ПАП-теста были отклонения, обнаруженные с помощью TS (2,8%); у двух из трех женщин с ASCUS (66,7%) и двух из четырех женщин с LSIL (50%) были отклонения, обнаруженные с помощью прибора TS, и ни одна из пациенток с эндометриальными клетками не имела отклоняющихся от нормы результатов TS.
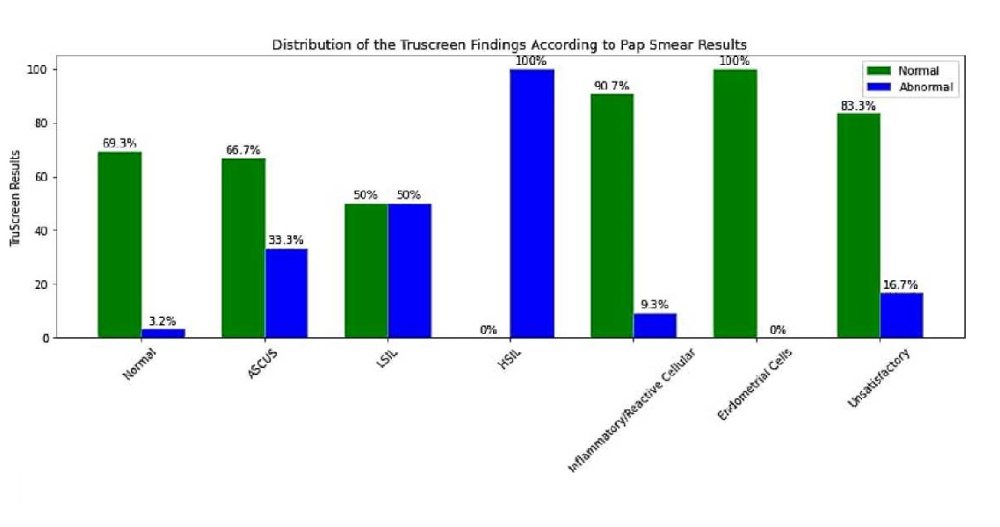
Сокращения: ASCUS: атипические клетки плоского эпителия неясного значения, HSIL: плоскоклеточные интраэпителиальные поражения высокой степени, LSIL: плоскоклеточные интраэпителиальные поражения низкой степени.
Кольпоскопию прошли 30 женщин, из них у 13 (43,3%) были выявлены поражения низкой степени, и только у одной (3,3%) - поражения высокой степени. У девяти женщин (30%) наблюдался сосудистый рисунок, в то время как ни у одной из них не было микроинвазии.
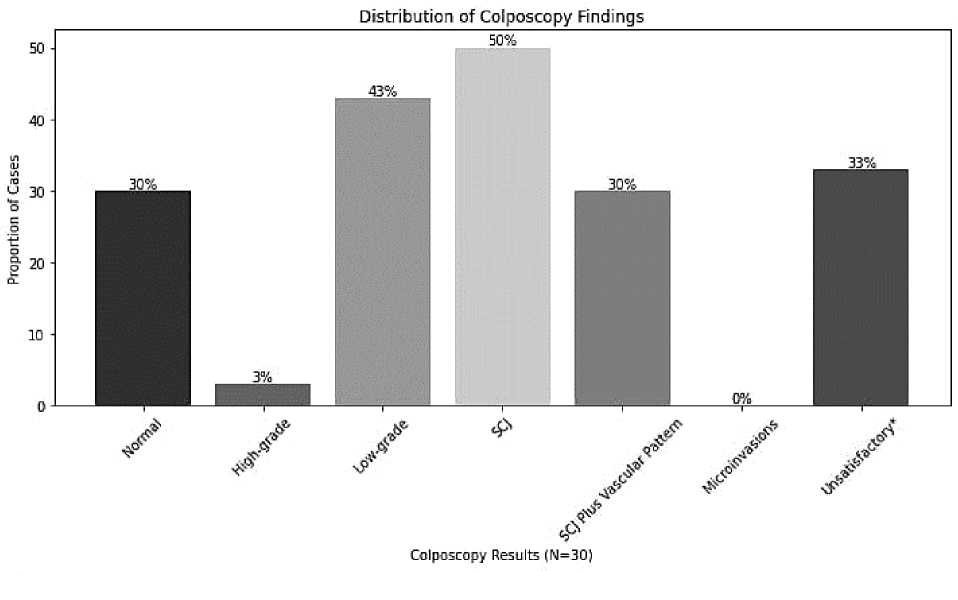
Распределение
результатов кольпоскопии
*
Неудовлетворительные результаты
кольпоскопии указывают на невозможность
визуализации плоско-столбчатого
соединения.
Сокращения:
SCJ:
плоско-столбчатое соединение.
Что касается результатов биопсии, у трех женщин была выявлена цервикальная интраэпителиальная неоплазия (CIN I), у двух - рак шейки матки (CIN II+) и у одной - железистая гиперплазия.
Эффективность скрининга с помощью TruScreen и ПАП-теста
Предел чувствительности TS составил 83,3% (95% доверительный интервал (ДИ): 35,9% - 99,6%) и специфичность 95% (95% доверительный интервал (ДИ): 92,7% - 96,8%) для выявления патологически диагностированных новообразований шейки матки по сравнению с 66,7% (95% ДИ: 22,3% - 95,7%) и 98,2% (95% ДИ: 96,6% - 99,2%) для ПАП-теста, соответственно. Разница между двумя инструментами скрининга не была статистически значимой (p = 0,91). Для женщин с CIN I чувствительность TS составила 66,7% (95% ДИ: 12,5% - 98%), а специфичность - 95,6% (95% ДИ: 93,4% - 97,2%), по сравнению с 66,7% (95% ДИ: 12,5% - 98%) и 98,2% (95% ДИ: 96,6% - 99,2%) для ПАП-теста, соответственно. Для поражений CIN II+ чувствительность (100%; 95% ДИ 15,8% - 100%) и специфичность (95,6%; 95% ДИ 93,4% - 97,2%) TS и чувствительность (100%; 95% ДИ 15,8% - 100%) и специфичность (98,6%; 95% ДИ 97,1 - 99,4%) ПАП-теста были высокими. В отношении железистой гиперплазии (Таблица 2) не было выявлено значительной разницы в результатах скрининга TS и ПАП-теста.
При сочетании TS и ПАП-теста были получены следующие диагностические параметры: для патологически диагностированных новообразований шейки матки чувствительность составила 100% (95% ДИ: 54,1% - 100%), а специфичность - 99,8% (95% ДИ: 98,89% - 99,9%). Для женщин с CIN I чувствительность составила 100% (95% ДИ: 54,1% - 100%), а специфичность - 99,8% (95% ДИ: 98,89% - 99,99%). В то время как для поражений CIN II+ чувствительность составила 100% (95% ДИ: 54,1% - 100%), а специфичность - 99,80% (95% ДИ: 98,89% - 99,99%).
Таблица 2: Эффективность скрининга с помощью прибора TruScreen и ПАП-теста
Статистика |
TruScreen |
ПАП-тест |
Комбинация ПАП-теста + Truescreen |
Значение Р* |
||||||
Нет / итого |
Значение |
95% ДИ |
Нет / итого |
Значение |
95% ДИ |
Нет / итого |
Значение |
95% ДИ |
||
Выявление случаев отклонения от нормы (n=6) |
||||||||||
Чувствительность |
5/6 |
83,3% |
35,9 к 99,6% |
4/6 |
66,7% |
22,3% к 95,7% |
6/6 |
100% |
54% r 100% |
0,910# |
Специфичность |
476/501 |
95% |
92,7% к 96,8% |
492/501 |
98,2% |
96,6% к 99,2% |
500/501 |
99,80% |
98,89% к 99,99% |
|
Положительная предсказательная ценность (PPV) |
5/5 |
100% |
54,1% к 100% |
4/4 |
100% |
54,1% к 100% |
5/5 |
100% |
54,1% к 100% |
|
Отрицательная предсказательная ценность (NPV) |
467/467 |
100% |
54,1% к 100% |
492/492 |
100% |
54,1% к 100% |
500/500 |
100% |
54,1% к 100% |
|
Обнаружение CIN I (n =3) |
||||||||||
Чувствительность |
2/3 |
66,7% |
12,5 - 98% |
2/3 |
66,7% |
12,5 - 98% |
3/3 |
100% |
54,1% к 100% |
|
Специфичность |
476/498 |
95,6% |
93,4% к 97,2% |
492/501 |
98,2% |
96,6% к 99,2% |
500/501 |
99,80% |
98,89% к 99,99% |
|
Положительная предсказательная ценность (PPV) |
2/2 |
100% |
20,0% к 100% |
2/2 |
100% |
20 - 100% |
3/3 |
100% |
54,1% к 100% |
|
Отрицательная предсказательная ценность (NPV) |
467/467 |
100% |
54,1% к 100% |
492/492 |
100% |
54,07% к 100% |
500/500 |
100% |
54,1% к 100% |
|
CIN II+ (n =2) |
||||||||||
Чувствительность |
2/2 |
100% |
15,81% к 100% |
2/2 |
100% |
15,8% к 100% |
2/2 |
100% |
54,1% к 100% |
|
Специфичность |
476/499 |
95,3% |
93,2% к 97,1% |
492/499 |
98,6% |
97,1% к 99,4% |
500/501 |
99,80% |
98,89% к 99,99% |
|
Положительная предсказательная ценность (PPV) |
1/1 |
100% |
15,8% к 100% |
1/1 |
100% |
15,8% к 100% |
2/2 |
100% |
54,1% к 100% |
|
Отрицательная предсказательная ценность (NPV) |
467/467 |
100% |
54,07% к 100% |
492/492 |
100% |
54,07% к 100% |
500/500 |
100% |
54,1% к 100% |
|
Железистая гиперплазия (n=1) |
||||||||||
Чувствительность |
1/1 |
100% |
5,5 к 100% |
0/1 |
0% |
0% к 94% |
1/1 |
100% |
54,1% к 100% |
0,761 |
Специфичность |
476/500 |
95,2% |
92,9 % к 96,9% |
492/500 |
98,4% |
96,8% к 99,3% |
500/501 |
99,80% |
98,89% к 99,99% |
|
Положительная предсказательная ценность (PPV) |
1/1 |
100% |
5,5 к 100% |
0/1 |
0% |
0% к 94% |
1/1 |
100% |
54,1% к 100% |
|
Отрицательная предсказательная ценность (NPV) |
467/467 |
100% |
54,1% к 100% |
492/492 |
100% |
54,1% к 100% |
500/500 |
100% |
54,1% к 100% |
|
#Тест хи-квадрат или точный тест Фишера; * для Truscreen по сравнению с ПАП-тестом
Рассмотрение полученных результатов
В последние годы в ряде развитых стран отмечается значительное снижение заболеваемости и смертности от рака шейки матки благодаря внедрению национальных протоколов скрининга [27, 28]. Тем не менее, заболеваемость и смертность от рака шейки матки в ближневосточном регионе являются значительными и возросли за период с 2000 по 2017 год [29]. Хотя такой рост можно объяснить улучшением доступа к медицинским услугам и изменением образа жизни [29], предыдущие отчеты указывают на то, что неоптимальная реализация программ скрининга и отсутствие обученного персонала также являются основными факторами [30].
Хотя цитология считается основным инструментом скрининга в странах Ближнего Востока, включая Саудовскую Аравию, она имеет ряд недостатков, которые включают в себя необходимость забора образца шейки матки, наличия лабораторного оборудования и квалифицированных цитопатологов. Все это ограничивает доступность цитологии для людей, проживающих в сельских районах и в условиях ограниченных ресурсов. Кроме того, в некоторых регионах мира использование ПАП-теста может быть неприемлемым с точки зрения культуры [31-33]. Поэтому существует потребность в существовании более практичного, но точного инструмента для скрининга рака шейки матки. TS может обеспечить быструю и практичную оценку новообразований шейки матки путем измерения затухания напряжения на различных частотах в тканях шейки матки [19]. Хотя TS не может определить степень патологии, растущее число доказательств свидетельствует о том, что TS обладает высокой эффективностью в выявлении новообразований шейки матки [34]. Сравнительное исследование TS и обычного ПАП-теста в больнице Уиттингтон в Лондоне показало, что TS ассоциируется со значительно меньшей болью, давлением и соскабливанием по сравнению со шпателем или щеточкой, используемыми для сбора клеточного материала с шейки матки при цитологическом скрининге [23]. Кроме того, женщины предпочитали получать результат незамедлительно [23].
Настоящее исследование показало, что TS в режиме реального времени обладает высокой чувствительностью (83,3%) и специфичностью (95%) для выявления неоплазии шейки матки, что сопоставимо с результатами LBC. Скрининговая эффективность TS была одинаковой для CIN I, CIN II+ и поражений железистой гиперплазией (чувствительность от 66,7 до 100% и специфичность почти 96%). Кроме того, TS показал высокий показатель PPV, что подчеркивает его роль в снижении затрат, связанных со скринингом, за счет уменьшения числа женщин, которые без необходимости подвергаются кольпоскопии и биопсии. Кроме того, наши результаты показали, что частота положительных результатов TS заметно возрастала с увеличением тяжести поражения.
Наши результаты согласуются с результатами предыдущего проспективного исследования, показавшего, что чувствительность и NPV TS для выявления патологий шейки матки составляют 86,1% и 89,5% соответственно [34]. Более того, в одном из недавних отчетов было показано, что чувствительность и специфичность TS для выявления CIN II+ у ВПЧ-положительных пациенток составляют 96,3% и 46,4% соответственно [20]. В предыдущем метаанализе чувствительность и специфичность TS составили 76% и 69% соответственно [35].
Другие отчеты показали более низкую чувствительность TS, чем наши результаты. Например, Кампос и соавторы сообщили о чувствительности в 43% для выявления внутриэпителиальных поражений высокой степени. Тем не менее, исследование показало хорошую согласованность между TS и кольпоскопией [19]. Такое расхождение в опубликованной литературе может быть связано с различиями в обследуемой популяции, стандартным методом выявления и/или методологическими различиями при расчете эффективности скрининга TS.
В литературе все чаще встречаются данные о том, что сочетание TS с другими методами позволяет повысить точность и снизить необходимость в кольпоскопии. Wei и соавторы сообщили, что TS имеет более высокую чувствительность и специфичность, чем ПАП-тест. Тем не менее, когда эти два метода были скомбинированы, чувствительность и специфичность возросли [22], что согласуется с нашими результатами. Наибольшую чувствительность (96,3%) и специфичность (83,6%) для CIN II+ показала комбинация HPV16/18 и TS (оба положительные) [20].
В недавнем исследовании тест на жидкостную тонкослойную цитологию (ТСТ) в сочетании с ВПЧ имел значительно меньшую специфичность (39,9%), чем ВПЧ в сочетании с TS (50%) для CIN II+ у женщин с высоким риском положительного ВПЧ, в то время как чувствительность для этих двух комбинаций была сопоставимой (93,94% против 87,88%). Аналогичная картина наблюдалась и у пациентов с CIN III+ [22]. Таким образом, комбинация TS и ВПЧ обладает отличным потенциалом для эффективного скрининга рака шейки матки. Исследования, проведенные в Китае, Польше и Турции, показали аналогичные результаты [24]. Однако для анализа и проверки достоверности этого вывода необходимы дополнительные данные.
Насколько известно, наше исследование представляет собой первичные данные из ближневосточного региона о целесообразности и эффективности скрининга с помощью TS для выявления новообразований шейки матки. Преимуществом настоящего исследования является проспективный сбор данных, что позволяет избежать ошибки классификации или предвзятости при установлении диагноза. К ограничениям относится то, что объем выборки, особенно среди женщин, получивших направление на кольпоскопию, был относительно небольшим (некоторые из них не захотели проводить исследование, а некоторые его прекратили), что может увеличить вероятность ошибки второго типа. Несмотря на то, что три больницы расположены в Эр-Рияде, пациенты приезжали со всего Королевства, так как данные учреждения являются специализированными. В будущем рекомендуется проводить исследования на большем количестве образцов по всей стране, чтобы подтвердить результаты данного исследования в более широком масштабе на примере разных регионов и групп населения с разным социально-экономическим положением.
Заключение
TS представляет собой надежный и практичный инструмент скрининга новообразований шейки матки, не требующий взятия образцов шейки матки, наличия лабораторного оборудования и обученного персонала. Несмотря на то, что в ходе нашего исследования обследования проводились врачами, медсестры также могут быть обучены и участвовать в скрининговых программах, чтобы самостоятельно проводить TS-обследование. Наше исследование показало, что инструмент обеспечивает точные результаты скрининга в режиме реального времени, что делает его пригодным для быстрого обследования женщин из группы риска или в условиях ограниченных ресурсов. Кроме того, это может послужить толчком к переходу на протокол "осмотр и лечение", поскольку появляется все больше доказательств в пользу такого подхода.
Полученные нами результаты могут послужить основой для разработки политики для выбора оптимальной стратегии скрининга рака шейки матки в странах, не имеющих установленной национальной программы скрининга. Однако для подтверждения клинической эффективности TS у жителей Ближнего Востока необходимы дополнительные исследования.
Заявления
Заявление о финансировании:
Авторы не получали финансовой поддержки для исследования, авторства и/или публикации этой статьи.
Заявление о конфликте интересов:
Все авторы заявляют об отсутствии конфликта интересов.
Благодарности:
Авторы выражают благодарность следующим коллегам за уделенное время и самоотверженный труд в течение всего периода исследования:
Dr.
Shehnaz Iqbal, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr.
Shakera Parveen, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr.
Suhad AlKaf, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Ranya AbdelJabbar, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Shaza Yassin, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Thana Goda, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Nabeela Abu Tahoun, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Aida Saeed, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Gina Aboutaleb, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Majdolin Yahya, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Salwa Ibrahim, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Huwaida Elattia, Consultant OBGYN, Dr Sulaiman Alhabib Medical Group
Dr. Naf a Chaudhry, Specialist OBGYN, Dr Sulaiman Alhabib Medical Group
Авторский вклад:
Доктор Маджед Альхуд (Majed Alhudhud) разработал концепцию и дизайн анализа, доктор Мааб Эль Хуссиен (Maab El Hussien) занимался сбором данных. Остальные авторы предоставили данные и инструменты для анализа, а также участвовали в привлечении пациентов. Кроме того, доктор Мааб Эльхуссиен (Maab El Hussien) выполнил анализ, а доктор Маджед Альхуд (Majed Alhudhud) написал рукописный документ.
Заявление об использовании данных:
Будут ли доступны индивидуальные данные участников (включая словари базы данных)? |
Да |
Какие именно данные будут доступны? |
Индивидуальные данные участников, которые лежат в основе результатов, представленных в этой статье, после деидентификации (текст, таблицы, рисунки и приложения). |
Какие еще документы будут в доступе? |
Протокол исследования |
Когда будут доступны данные (даты начала и окончания предоставления доступа)? |
Время начала предоставления доступа к данным - через 9 месяцев и до 36 месяцев с момента публикации статьи. |
Кому? |
Исследователям, предполагаемое использование ими данных было одобрено независимым комитетом, созданным для этой цели. |
Для какого вида анализа? |
Для мета-анализа данных по отдельным участникам. |
С помощью какого механизма будет осуществляться передача данных? |
Предложения могут быть поданы в течение 36 месяцев после публикации статьи. Через 36 месяцев данные будут доступны в хранилище данных Исследовательского центра нашего больничного учреждения без исследовательской поддержки, за исключением депонированных метаданных. |
Ссылки
Ferlay J, Soerjomataram I, Dikshit R, et al. Заболеваемость раком и смертность от рака в мире: источники, методы и основные закономерности в GLOBOCAN 2012 (Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012). Int J cancer 2015; 136: E359-E386.
Sung H, Ferlay J, Siegel RL, et al. Глобальная статистика рака 2020: ГЛОБОКАН Оценка заболеваемости и смертности в мире по 36 видам рака в 185 странах (Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries). CA Cancer J Clin 2021; 71: 209-249.
Siegel R, Ma J, Zou Z, et al. Статистика раковых заболеваний, 2014 год (Cancer statistics, 2014).
CA Cancer J Clin 2014; 64: 9-29.
Mandelblatt JS, Lawrence WF, Gaffikin L, et al. Затраты и преимущества различных стратегий скрининга рака шейки матки в менее развитых странах (Costs and Benefits of Different Strategies to Screen for Cervical Cancer in Less-Developed Countries). JNCI J Natl Cancer Inst 2002; 94: 1469-1483.
Allameh T, Khanjani S, Mohammadizadeh F, et al. Диагностическая ценность комбинации TruScreen и ПАП-теста при скрининге эпителиальных поражений шейки матки: Имеет ли данный метод преимущества только перед ПАП-тестом? (Diagnostic value of the combination of TruScreen and Pap smear in screening cervical epithelial lesions: Does it add advantages over the Pap smear alone?). Open J Obstet Gynecol 2013; 03: 341-346.
Munoz N, Bosch FX, de Sanjose S, et al. Эпидемиологическая классификация типов вируса папилломы человека, ассоциированных с раком шейки матки (Epidemiologic Classification of Human Papillomavirus Types Associated with Cervical Cancer). N Engl J Med 2003; 348: 518-527.
Matsumoto K, Oki A, Furuta R, et al. Прогнозирование прогрессирования предыдущих цервикальных поражений с помощью генотипирования вируса папилломы человека: проспективное когортное исследование (Predicting the progression of cervical precursor leisons by human papillomavirus genotyping: a prospective cohort study). Int J cancer 2011; 128: 2898-2910.
HolowatyP MillerAB, Rohan T, etal. Естественная история дисплазии шейки матки (Natural Historyof Dysplasia ofthe Uterine Cervix). JNCIJ Natl Cancer Inst 1999; 91: 252-258.
Dorji N, Tshering S, Choden S, et al. Оценка диагностической эффективности кольпоскопии в диагностике гистологической цервикальной интраэпителиальной неоплазии 2+ (CIN2+) (Evaluation of the diagnostic performance of colposcopy in the diagnosis of histologic cervical intraepithelial neoplasia 2+ (CIN2+). BMC Cancer 2022; 22: 930.
Stefan DC, Dangou JM, Barango P, et al. Задача по ликвидации рака шейки матки к 2030 году: базовая оценка ситуации в шести странах Африки- часть II (Targeting elimination of cervical cancer by 2030: a baseline assessment in six African countries—part II). Ecancermedicalscience; 16. Epub ahead of print 2022. DOI: 10.3332/ECANCER.2022.1454.
Nations U. 70/1. Преобразование нашего мира: Повестка дня на период до 2030 года по устойчивому развитию (Transforming our world: the 2030 Agenda for Sustainable Development).
Всемирная организация здравоохранения. Глобальная стратегия по ускорению ликвидации рака шейки матки как проблемы общественного здравоохранения и связанные с ней цели и задачи на период 2020 - 2030 гг. (Global strategy to accelerate the elimination of cervical cancer as a public health problem and its associated goals and targets for the period 2020 - 2030). Генеральная Ассамблея ООН 2020; 2: 1-56.
Lazcano-Ponce E, Palacio-Mejia LS, Allen-Leigh B, et al. Снижение смертности от рака шейки матки в Мексике: Влияние распространения ПАП-тестов, уровня рождаемости и важности диагностической валидности цитологии (Decreasing Cervical Cancer Mortality in Mexico: Effect of Papanicolaou Coverage, Birthrate, and the Importance of Diagnostic Validity of Cytology). Cancer Epidemiol Biomarkers Prev 2008; 17: 2808-2817.
Dorji N, Tshering S, Choden S, et al. Оценка диагностической эффективности кольпоскопии в диагностике гистологической цервикальной интраэпителиальной неоплазии 2+ (CIN2+) (Evaluation of the diagnostic performance of colposcopy in the diagnosis of histologic cervical intraepithelial neoplasia 2+ (CIN2+). BMC Cancer; 22. Epub ahead of print 1 December 2022. DOI: 10.1186/S12885-022-10030-7.
Barut MU, Kale A, Kuyumcuoglu U, et al. Анализ чувствительности, специфичности, положительной и отрицательной предсказательной ценности ПАП-теста и кольпоскопии в диагностике предраковых и злокачественных поражений шейки матки (Analysis of Sensitivity, Specificity, and Positive and Negative Predictive Values of Smear and Colposcopy in Diagnosis of Premalignant and Malignant Cervical Lesions). Med Sci Monit 2015; 21: 3860.
Louwers J, Kocken M, ter Harmsel W, et al. Цифровая кольпоскопия: готова ли она к использованию? (Digital colposcopy: ready for use?) Обзор литературы. BJOG An Int J Obstet Gynaecol 2009; 116: 220-229.
Sauvaget C, Fayette J-M, Muwonge R, et al. Точность визуального осмотра с помощью уксусной кислоты для скрининга рака шейки матки (Accuracy of visual inspection with acetic acid for cervical cancer screening). Int J Gynecol Obstet 2011; 113: 14-24.
Bedell SL, Goldstein LS, Goldstein AR, et al. Скрининг рака шейки матки: Прошлое, настоящее и будущее (Cervical Cancer Screening: Past, Present, and Future). Sex Med Rev2020; 8: 28-37.
Salazar-Campos J, Gonzalez-Enciso A, D^az-Molina R, et al. Скрининг рака шейки матки - TruScreen™ в сравнении с традиционной цитологией: Пилотное исследование (Cervicouterine cancer screening - TruScreen™ vs. conventional cytology: Pilot study). J Cytol 2018; 35: 143.
Wang Z, Kang Y, Yu F, et al. Обследование тканей шейки матки с помощью прибора TruScreen у женщин, инфицированных вирусом папилломы человека с высокой степенью риска, во время пандемии COVID-19 (TruScreen detection of cervical tissues for high-risk human papillomavirus-infected women during the COVID-19 pandemic). Futur Oncol 2021; 17: 1197-1207.
Ma Y, Di J, Bi H, et al. Сравнение частоты выявления поражений шейки матки с помощью прибора TruScreen, LBC-теста и ВПЧ-теста: Реальное исследование на основе скрининга рака шейки матки в сельских районах Китая (Comparison of the detection rate of cervical lesion with TruScreen, LBC test and HPV test: A Real-world study based on population screening of cervical cancer in rural areas of China). PLoS One 2020; 15: e0233986.
Wei Y, Wang W, Cheng M, et al. Клиническая оценка оптико-электронного устройства реального времени для скрининга рака шейки матки. Eur J Obstet Gynecol Reprod Biol 2021; 266: 182-186.
Singer A, Coppleson M, Canfell K, et al. Оптоэлектронное устройство для обследования в режиме реального времени в качестве дополнения к ПАП-тесту для скрининга шейки матки: Многоцентровая оценка (A real time optoelectronic device as an adjunct to the Pap smear for cervical screening: A multicenter evaluation). Int J Gynecol Cancer 2003; 13: 804-811.
Noel-Storr AH, McCleery JM, Richard E, et al. Стандарты отчетности для исследований точности диагностических тестов при деменции: Инициатива STARDdem (Reporting standards for studies of diagnostic test accuracy in dementia: The STARDdem Initiative). Neurology 2014; 83: 364-373.
Pangarkar MA. Система отчетности по цервикальной цитологии Bethesda (The Bethesda System for reporting cervical cytology). Cytojournal 2022; 19: 28.
cervical-screening-histopathology-reporting-handbook/cervical-screening-programme-histopathology-reporting- guidance#terminology.
ВОЗ. Комплексный контроль рака шейки матки. Руководство по основной практике. Второе издание (WHO. Comprehensive Cervical Cancer Control A guide to essential practice Second edition. Comprehensive Cervical Cancer Control A guide to essential practice Second edition).
AIHW. Цервикальный скрининг в Австралии в 2019 году, краткое содержание - Австралийский институт здравоохранения и социального обеспечения. Австралийский институт здравоохранения и социального обеспечения (Cervical screening in Australia 2019, Summary - Australian Institute of Health and Welfare. Australian Institute of Health and Welfare).
Safaeian F, Ghaemimood S, El-Khatib Z, et al. Заболеваемость раком шейки матки в регионе Восточного Средиземноморья в 2000 и 2017 годах: Ретроспективный анализ данных Глобального исследования заболеваемости (Burden of Cervical Cancer in the Eastern Mediterranean Region During the Years 2000 and 2017: Retrospective Data Analysis of the Global Burden of Disease Study). JMIR Public Heal Surveill 2021; 7: e22160.
Alhamlan FS, AlAhdal MNA, Al-Zahrani AS, et al. Вирусы папилломы человека: Рассказ о раке шейки матки в развивающихся странах (Human papillomaviruses: The cervical cancer saga in developing countries). J Infect Dev Ctries 2017; 11: 819-825.
Nikumbh DB, Nikumbh RD, Kanthikar SN. Ограничения цитологического скрининга рака шейки матки (ПАП-тест) в сельской местности Индии в разрезе технических и культурных аспектов (Limitations of cytological cervical cancer screening (Papanicolaou test) regarding technical and cultural aspect in rural India). South Asian J Cancer 2016; 05: 079-079.
Boone JD, Erickson BK, Huh WK. Новые взгляды на скрининг рака шейки матки (New insights into cervical cancer screening). J Gynecol Oncol 2012; 23: 282.
Nasser H, AlAyyaf M, Atallah A, et al. Одиннадцатилетний обзор данных о ПАП-тестах в Саудовской Аравии: нужно уделять больше внимания аномалиям желез! (Eleven-year review of data on Pap smears in Saudi Arabia: We need more focus on glandular abnormalities!) Ann Saudi Med 2017; 37: 265-271.
Ozgu E, Yildiz Y, Salman Ozgu B, et al. Эффективность оптико-электронного прибора реального времени (TruScreenTM) в выявлении интраэпителиальных патологий шейки матки: проспективное обсервационное исследование (Efficacy of a real time optoelectronic device (TruScreenTM) in detecting cervical intraepithelial pathologies: a prospective observational study). J Turkish Ger Gynecol Assoc 2015; 16: 41-44.
Yang H, Zhang X, Hao Z. диагностическая точность оптико-электронного прибора реального времени при скрининге рака шейки матки. Медицина (Балтимор) (The diagnostic accuracy of a real-time optoelectronic device in cervical cancer screening. Medicine (Baltimore)) 2018; 97: e11439.
