Частота выявления поражения шейки матки с помощью TruScreen, LBC-теста и ВПЧ-теста в сельских районах Китая
Сравнение частоты выявления поражения шейки матки с помощью TruScreen, LBC-теста и ВПЧ-теста: Реальное исследование на основе популяционного скрининга рака шейки матки в сельских районах Китая
Аннотация
Предпосылки и цель Китай несет тяжелое бремя рака шейки матки и имеет тревожно низкий уровень скрининга рака шейки матки. Для достижения цели ликвидации рака шейки матки в Китае срочно необходимы соответствующие методы и стратегии.
Материалы и методы
В этом исследовании приняли участие 9972 женщины, прошедшие скрининг рака шейки матки в рамках Национальной программы скрининга рака шейки матки в сельской местности (NCCSPRA) в 8 проектных уездах. Всем участницам были проведены TruScreen, ВПЧ-тест и LBC-тест. В общей сложности 1945 женщин с одним или более чем одним положительным или аномальным результатом трех вышеперечисленных скрининговых тестов впоследствии прошли кольпоскопию. Сравнивалась частота выявления CIN2+ между тремя тестами.
Результаты
Независимо от того, какой метод скрининга используется, частота выявления CIN2+ в восточных
регионах была намного выше, чем в центральных и западных. Общая частота выявления
CIN2+ в группе ВПЧ был самой высокой (0,73%), затем в группе LBC (0,44%) и TS группа (0,31%). Имелась статистически значимая разница в общей частоте выявления CIN2+ между группами TS и HPV, LBC и HPV, соответственно. Статистической разницы в общей частоте выявления CIN2+ между группами скрининга TS и LBC не было. Кроме того, за исключением восточных регионов, не было статистической разницы в частоте выявления CIN2+ между группой TS и двумя другими группами в центральных и западных регионах.
Заключение
Тест на ВПЧ, по-видимому, является предпочтительным методом скрининга рака шейки матки в сельских районах Китая. Такие характеристики, как минимальные требования к обучению, простота эксплуатации, получение результатов в режиме реального времени без сбора образцов клеток шейки матки и помощи лабораторного оборудования и специалистов, делают TS идеальным для скрининга рака шейки матки в регионах с низкими ресурсами.
Введение
Во всем мире рак шейки матки ежегодно поражает более полумиллиона женщин и убивает четверть миллиона [1]. Если не принять меры, то к 2030 году смертность от рака шейки матки возрастет почти на 50 % [2]. Из-за большой численности населения Китай несет тяжелое бремя рака шейки матки. Между тем существуют очевидные региональные различия в заболеваемости и смертности от рака шейки матки в Китае, а заболеваемость и смертность от рака шейки матки имеют тенденцию к росту с 2000 года [3, 4]. В 2009 году с целью снижения высокого уровня рака шейки матки в сельских районах правительство Китая запустило Национальную программу скрининга рака шейки матки в сельских районах (NCCSPRA) [5].
Однако существовал ряд слабых мест и угроз [6] - нехватка персонала для интерпритации цитологических препаратов, ограниченные возможности медицинских учреждений в отдаленных и бедных районах, большое количество населения для скрининга - которые мешали реализации программы скрининга и создавали проблемы для надлежащего скрининга на основе популяции, особенно в центральных и западных регионах [7]. В 2018 году ВОЗ выступила с глобальным призывом к действиям по ликвидации рака шейки матки и поставила цель к 2030 году обеспечить 70 % женщин, прошедших скрининг с помощью высокоточного теста в возрасте 35 и 45 лет [1]. Однако в настоящее время в Китае отмечается тревожно низкий уровень скрининга рака шейки матки (26,7 %) среди женщин в возрасте 35-64 лет [8]. Таким образом, для достижения цели ликвидации рака шейки матки в Китае необходимо срочно изучить и оценить инновационные методы скрининга.
Искусственный интеллект (ИИ) стремительно развивается в последние годы и оказывает далеко идущее влияние на скрининг рака шейки матки. Одним из методов ИИ, вызвавшим интерес медицинских работников в этой области, является TruScreen (TS) (Polarprobe; Polartechnics, Австралия), который использует оптическую и электрическую стимуляцию для выявления рака и предраковых заболеваний в тканях шейки матки, причем он работает в режиме реального времени и является не инвазивным [9].
Однако, в настоящее время большинство исследований, посвященных скринингу рака шейки матки с помощью TS, основаны на небольших выборках клинических пациентов, а оценка скринингового эффекта TS в разных исследованиях сильно различается. Некоторые исследования показали, что эффект TS соответствует эффекту цитологии, но некоторые исследования показывают, что его скрининговый эффект не так хорош, как у цитологического исследования [10-12]. Так есть ли в реальном мире разница в частоте выявления поражения шейки матки между TS и тестом на вирус папилломы человека (ВПЧ) и жидкостной цитологией (LBC), которые в настоящее время используются в проектной группе NCCSPRA? Что подходит для скрининга рака шейки матки на массовом уровне в Китае? Все эти вопросы заслуживают нашего дальнейшего изучения на больших выборках, в многоцентровых центрах и в рамках популяционного скрининга.
Исследование в реальных условиях (RWS) - это исследование, в ходе которого собираются разнообразные данные в реальной клинической, общественной или научной среде [13]. RWS имеет следующие характеристики: широкий охват, обычно большой размер выборки; распределение по группам основано на добровольном участии или клиническом выборе, не обязательно рандомизированном. Результаты оценки RWS основаны на реальной, статистически достоверной оценке и достаточной доказательной базе [14]. Настоящая цель исследования - обобщить результаты диагностики и лечения реальных клинических случаев, чтобы сделать данные исследования более применимыми для практической работы [15].
Это исследование основано на изучении реальных условий жизни людей, прошедших скрининг рака шейки матки, проведенный местным персоналом в рамках проекта по скринингу рака шейки матки в сельской местности Китая. Цель данного исследования - подвести научную основу для разработки стратегии скрининга рака шейки матки, соответствующей реальной ситуации в нашей стране.
Материалы и методы
Участники и процедуры
Данное исследование проводилось с августа по декабрь 2018 года. Учитывая влияние экономического развития и географического положения на заболеваемость и эффективность скрининга рака шейки матки, был принят многоступенчатый метод выборки для разделения страны на 3 региона (восточный, центральный и западный) в соответствии с географическим положением и уровнем экономического развития. Два из четырех регионов-участников проекта NCCSPRA использовали тест LBC в качестве метода скрининга в восточном (район Хайдиан в Пекине, уезд Лоюань в провинции Фуцзянь), центральном (Заоян в Хубэ) и западном регионах (Цзаоян в провинции Хубэй, уезд Пинцзян в провинции Хунань) и западных регионах (Алетай в Синьцзян-Уйгурском автономном районе, уезд Дэян в провинции Сычуань, уезд Хэчуань в Чунцине, уезд Ханьчэн в провинции Шэньси) соответственно, были выбраны в качестве районов исследования.
В исследование было включено 10 024 женщины, прошедшие процедуры скрининга рака шейки матки в рамках проекта NCCSPRA в 8 округах. В исследование были включены женщины с неизмененной шейкой матки, без заболеваний шейки матки в анамнезе, без биопсии шейки матки, микроволнового, лазерного, лучевого и химиотерапевтического лечения в течение 3 месяцев. Женщины с сильным неконтролируемым кровотечением из шейки матки, женщины, отказавшиеся от участия в исследовании, не способные соблюдать процедуры исследования, страдающие фотосенсибилизацией или подвергшиеся фототерапии не включались в исследование.
Все участники дали письменное согласие на участие в данном исследовании и были проинформированы о мерах конфиденциальности и праве на отказ от участия. Данное исследование было одобрено Комитетом по этике Национального центра здоровья женщин и детей, Китайский ЦКЗ (No: FY2018-08).
С помощью структурированной анкеты информация о демографических характеристиках и истории болезни каждой женщины была получена до проведения клинического и лабораторного обследования квалифицированными исследователями. Всем женщинам был проведен гинекологический осмотр органов малого таза и скрининговое обследование TS, ВПЧ-тест (DH3, DALTONbio) и LBC-тест (D.A Diagnostics, Hologic, Kingmed Diagnostics). Порядок обследования и забора образцов был следующим: обследование TS, забор образцов LBC, забор образцов ВПЧ и осмотр таза. Женщины с положительным результатом TS, инфекцией ВПЧ 16/18 или аномальной цитологией (атипичные плоские клетки неопределенного значения, ASC-US+) были направлены на кольпоскопию.
Женщины с положительной инфекцией одного из 12 подтипов ВПЧ высокого риска (HPV 31,33,35,39,45,51,52,56,58,59,66 и 68) были направлены на LBC и TS. Женщинам с аномальными результатами кольпоскопии (поражение низкой степени, поражение высокой степени или с подозрением на рак) проводилась биопсия. Обследование TS, забор образцов LBC, забор образцов ВПЧ, кольпоскопия, биопсия, интерпретация цитологии и гистологии проводились местным персоналом, участвовавшим в NCCSPRA. Образцы ВПЧ были собраны единообразно и отправлены на исследование в определенные исследовательские учреждения. Кольпоскопия проводилась в соответствии с принятыми диагностическими стандартами и национальными рекомендациями. Биопсия, подтвердившая CIN2 + использовалась в качестве клинической конечной точки исследования.
Статистический анализ
Сравнение различных методов скрининга для выявления CIN2+ между группами использовался тест хи-квадрат Пирсона. Частота выявления CIN2+ = количеству выявленных случаев CIN2+ ÷ количество женщин, прошедших скрининг х 100 p<0,05 указывает на существенную разницу между группами, а p<0,017 указывает на существенную разницу между подгруппами.
Результаты
Всего 9972 женщины соответствовали критериям включения. Из 9972 участниц 2484 (24,9%) были из восточного региона, 2502 (25,1%) из центрального региона и 4986 (50,0%) из западного региона. Средний возраст участников составил 45,2±5,4 года. Общая распространенность положительных результатов TS, ВПЧ и LBC составила 12,2%, 7,5% и 3,1%, соответственно. Доля положительных результатов TS и LBC была наиболее высокой в восточных регионах (14,4% и 4,8%, соответственно). Доля положительных результатов ВПЧ в западных регионах была выше, чем в других регионах (Tаблица 1.)
В общей сложности 1945 (19,5%) женщин имели один или более одного положительного или аномального результата скрининга и нуждались в дальнейшей кольпоскопии. Среди них 96,8% (1882/1945) прошли кольпоскопию. Частота проведения кольпоскопии в центральном регионе была самой высокой (99,8%) (табл. 2).
Обсуждение
Некоторые развитые страны значительно снизили заболеваемость и смертность от рака шейки матки благодаря реализации национальных программ организованного скрининга [16, 17], однако в некоторых развивающихся странах (например, в Коста-Рике, Колумбии и Пуэрто-Рико) результаты оказались не столь позитивными [18, 19]. При сравнении эффективности программ скрининга рака шейки матки в разных странах выяснилось, что возможности медицинских учреждений в разных районах, количество цитологических приборов, условия проведения лабораторных исследований, а также уровень принятия и удовлетворенности населения методами скрининга оказывают влияние на эффективность широкомасштабного скрининга населения [20-22].
Поэтому с момента внедрения NCCSPRA в 2009 году исследователи занялись поиском метода скрининга рака шейки матки, который мог бы минимизировать вышеперечисленные отрицательно влияющие факторы и подходил бы для сельских районов Китая. В качестве основного метода скрининга, рекомендованного Национальной комиссией по здравоохранению (NHC) Китая, цитологический тест и тест на ВПЧ являются основными методами, используемыми для скрининга рака шейки матки в NCCSPRA [23, 24]. Как новый метод скрининга в режиме реального времени, некоторые исследования показали, что TS может стать еще одним более подходящим методом скрининга в развивающихся странах благодаря своим преимуществам: не инвазивности, мгновенной диагностике, снижению потребности в патоморфологах, портативности, а также схожей чувствительность и специфичность по сравнению с тестами на ВПЧ и LBC [25, 26].
Таблица 1. Положительные результаты скрининга на TS, ВПЧ и LBC в разных регионах Китая, 2018 г.
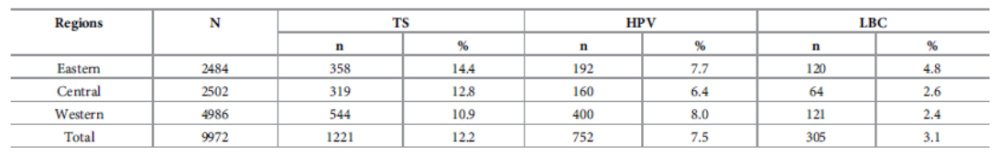
Таблица 2. Результаты проведения кольпоскопии и выявления CIN2+ в различных регионах Китая.
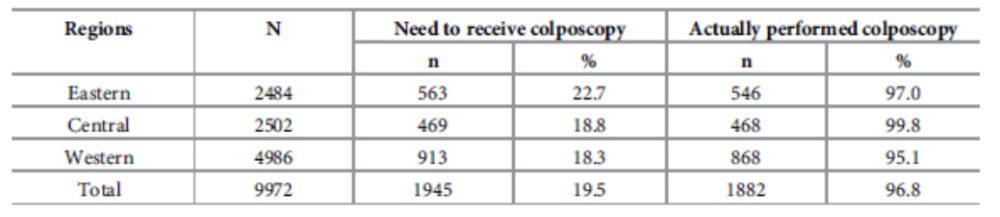
Таблица 3. Частота выявления CIN2+ в различных группах методов скрининга в разных регионах Китая.
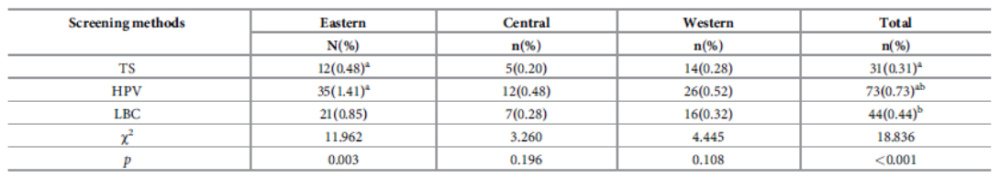
Вопрос о том, какой из вышеперечисленных методов больше всего подходит для программы скрининга рака шейки матки в сельских районах Китая. Поэтому данное исследование, основанного на реальных результатах, так особенно важено. Это первое многоцентровое крупномасштабное популяционное исследование, основанное на изучении реальных условий жизни людей, проходящих скрининг рака шейки матки на TS, ВПЧ и LBC, проведенное местным персоналом в рамках проекта скрининга рака шейки матки в сельской местности в Китае.
Результаты этого исследования показали, что независимо от того, какой метод скрининга используется, частота выявления CIN2+ в восточном регионе была намного выше, чем в центральном и западном регионах. Однако результаты отчета о заболеваемости и смертности от рака в различных районах Китая, 2014 [27] показали, что заболеваемость раком шейки матки в восточном регионе (мировые стандарты населения, ASIRW: 9,31/100 000) была ниже, чем в центральном (ASIRW: 12,25/100 000) и западном регионах (ASIRW: 10,51/100 000).
Результаты национальных исследований [6, 7] показали, что численность и возможности медицинского персонала в области цитологии и патологии в центральных и западных регионах были гораздо меньше и значительно ниже, чем в восточных регионах. Это еще раз доказывает, что независимо от метода скрининга, квалификация персонала и качество обслуживания являются очень важными факторами, влияющими на эффективность скрининга.
Результаты данного исследования показали, что общая частота выявления CIN2+ с помощью ВПЧ была самой высокой (0,73%), за ней следовали LBC (0,44%) и TS (0,31%). Более того, наблюдались статистически значимые различия в общей частоте выявления CIN2+ между TS и ВПЧ, а также LBC и ВПЧ, соответственно. Кроме того, ВПЧ-тест имеет следующие преимущества: простой процесс забора образцов, возможность самостоятельного забора образцов, автоматизированная обработка, высокая чувствительность и длительный интервал скрининга (5 лет) [28]. Это напоминает нам о том, что если он может соответствовать требованиям лаборатории и персонала, скрининг с помощью ВПЧ-теста представляется предпочтительным методом скрининга рака шейки матки, что согласуется с результатами предыдущего исследования, проведенного в Китае [29].
Еще одним важным результатом данного исследования является отсутствие статистической разницы в общей частоте выявления CIN2+ между группами скрининга TS и LBC. Более того, за исключением восточного региона, не было статистической разницы в частоте выявления CIN2+ между группой TS и двумя другими группами в центральном и западном регионах. В последние годы, благодаря возможности выбора и хорошей доступности, LBC постепенно вытесняет традиционный РАР-тест с шейки матки в качестве основного метода скрининга рака шейки матки. Однако, для проведения LBC требуется не только специальное оборудование и расходные материалы, но и подготовленные специалисты для интерпретации результата.
В отличие от цитологии, при TS исследуются не только поверхностные эпителиальные клетки. Свет на определенных частотах пропускается через ткань шейки матки, выявляя изменения в базальном и стромальном слоях, выявляя усиленнное кровообращение и изменения в клеточных ядрах и цитоплазме, которые возникают при предраковых изменениях [9]. Более того, по сравнению с цитологией и ВПЧ, TS не только обладает теми же преимуществами, что и ВПЧ-тест: простота обучения и эксплуатации, автоматическое формирование результатов, но и отличается тем, что результаты в режиме реального времени можно получить без забора образцов клеток шейки матки, без помощи лабораторного оборудования и цитологов [25]. Благодаря характеристикам TS и схожей с LBC частоте выявления CIN2+, TS может стать эффективным скрининговым тестом в тех регионах, где ВПЧ-тест не существует или не надежен.
В заключение следует отметить, что в целях выполнения глобального призыва к действиям по ликвидации рака шейки матки в 2019 году Госсовет Китая опубликовал документ "Здоровый Китай" (2019-2030), в котором указаны цели по скринингу рака шейки матки на период до 2030 года: к 2030 году скринингом рака шейки матки среди сельских женщин должно быть охвачено более 90% регионов Китая. При наличии большого количества людей, подлежащих скринингу, недостаток опытных цитологов и плохие лабораторные условия делают программу популяционного скрининга более сложной.
Высокая частота выявления CIN2+, минимальные требования к обучению, скорость анализа, автоматизированные функции ВПЧ-теста делают его идеальным для первичного скрининга шейки матки в регионах, где имеются соответствующие требования к лаборатории и персоналу для проведения ВПЧ-теста. Схожий с LBC эффект выявления и такие преимущества, как объективность и возможность проведения теста в режиме реального времени, делают TS альтернативным способом скрининга шейки матки в регионах с низкими ресурсами, где невозможно эффективно проводить цитологический скрининг, где отсутствуют условия для проведения ВПЧ-теста и трудности с наблюдением за пациентками, например, в центральных и западных регионах Китая.
Сильные стороны и ограничения
У данного исследования есть несколько сильных сторон: по сравнению с предыдущими исследованиями, данное исследование является первым крупномасштабным и популяционным исследованием TS-теста. За исключением ВПЧ-тестирования, все обследования и анализы проводились средним медицинским персоналом, участвовавшим в NCCSPRA. Это делает данное исследование основанным на реальных условиях при скрининге рака шейки матки. Все участницы данного исследования были обследованы одновременно тремя методами скрининга. Такая тактика позволяет избежать влияния на частоту выявления в различных скрининговых популяциях патологии шейки матки. Есть и некоторые ограничения данного исследования: Во многих округах проекта NCCSPRA, где для первичного скрининга использовался цитологический тест, частота проведения кольпоскопии составляла лишь 60%.
Однако в данном исследовании почти все пациентки (96,8%) с аномальными результатами скрининга прошли кольпоскопию, что может уменьшить преимущество TS в том, что можно сразу получить результаты и при необходимости провести кольпоскопию в тот же визит. В Китае многочисленное население и несбалансированное развитие. Данное исследование проводилось только в 8 районах Китая и может быть нерепрезентативным для остальной части страны. Однако, несмотря на эти ограничения, данное исследование в реальных условиях обеспечивает достоверность технологии скрининга и возможностей медицинского персонала в различных регионах, а также может служить доказательством для скрининга рака шейки матки в Китае и других развивающихся странах и регионах.
Благодарности
Выражаем признательность всем женщинам, принявшим участие в исследовании. Мы также выражаем благодарность всем сотрудникам, проводившим скрининг рака шейки матки и сбор данных в больницах MCH в Хайдиане, Лоюане, Заояне, Пинцзяне, Алетае, Дэяне, Хэчуане и Ханьчэне.
Авторский вклад
Курирование данных: Ю Ма.
Формальный анализ: Ю Ма.
Исследования: Цинпин Чжао, Тяньхуа Цинь, Вэнь Сюй, Чжаоян Лю, Няньхуа И, Цзин Чжао, Депин Чжоу, Цзянькуй Чэнь.
Методология: Цзянли Ди.
Управление проектом: Цзянли Ди.
Наблюдение: Jiangli Di, Qi Yang.
Написание - первоначального проекта: Юй Ма.
Написание - рецензирование и редактирование: Цзянли Ди, Хуэй Би.
Ссылки
- World Health Organization, Elimination of cervical cancer as a global health problem is within reach. Available from: https://www.who.int/reproductivehealth/topics/cancers/en/, accessed 15th, July 2019
- Cervical Cancer: An NCD We Can Overcome. Available from https://www.who.int/reproductivehealth/ DG_Call-to-Action.pdf?ua=1, accessed 15th, July 2019
- Hao J, Chen WQ, 2017 China Cancer Registration Annual report. People’s Health Publishing House. Beijing, 2018.
- Wei CH, Zhu JZ, Niu YN, Wang L, He JJ, Ma J, et al. Analysis of death trend of malignant tumors in female reproductive system in China from 2004 to 2016. Chinese Journal of Disease Control.2019; 23 (05): 506–511.
- MOH. Management Plan for Rural Areas Cervical Cancer and Breast Cancer Screening Examination Program. 2009. Available from: http://www.moh.gov.cn/fys/s7900/200906/ cd3c33a7ad624a50b8100b262041dabe.shtml, accessed 24th, June 2009
- Di JL, Opportunities and Challenges in Cervical Cancer Screening Program in China: SWOT Analysis for Implementation of Program.Quality in Primary Care. 2017; 25 (5): 282–288
- Ma L, Song B, Wu JL, Di JL, Zhao YX, Chen JY, et al. Analysis on the current situation of service capacity of two cancer screening program for rural women in China. Public Health in China.2018; 34 (09): 1250–1253.
- Bao HL, Zhang L, Wang LM, Zhang M, Zhao ZP, Fang LW, et al. Significant variations in the cervical cancer screening rate in China by individual-level and geographical measures of socioeconomic status: a multilevel model analysis of a nationally representative survey dataset. Cancer Medicine.2018; 7(5): 2089–2100. https://doi.org/10.1002/cam4.1321 PMID: 29573569 9. WHO, Cervical cancer Screening and treatmentof pre-cancerous lesionsfor secondary preventionof cervical cancerTechnology landscape, 2019.
- Pruski D, K´dzia W, Przybylski M, Jozefiak A, K´dzia H, Spaczyƒski M. The assesment of real optoelectronic method in the detection of cervical intraepithelial neoplasia. Ginekol Pol.2008; (79):342–346.
- O¨ zgu¨ E, Yildiz Y, O¨ zgu¨ BS, O¨ z M, Danışman UN, Gu¨ngo¨r T. Efficacy of a real time optoelectronic device (TruScreen™) in detecting cervical intraepithelial pathologies: a prospective observational study. Journal of the Turkish German Gynecological Association. 2015; 16(1):41–44. https://doi.org/10.5152/jtgga. 2015.15199 PMID: 25788849
- Salazar-Campos JE, Gonalez-Enciso A, Diaz-Molina R, Lara-Herna´ndez ME, Coronel-Martı´nez J, Pe´rez-Plasencia C, et al. Cervicouterine Cancer Screening—TruScreen vs. Conventional Cytology Pilot Study. Journal of Cytology. 2018.
- Sherman RE, Anderson SA, Dal Pan GJ, Gray GW, Gross T, Hunter NL, et al. Real-World Evidence— What Is It and What Can It Tell Us? The New England Journal of Medicine. 2016; 375(23):2293–2297. https://doi.org/10.1056/NEJMsb1609216 PMID: 27959688
- Chinese expert Committee on the implementation of Real-World Research in Clinical Medicine. Chinese Journal of Experimental and Clinical Infectious Diseases(Electronic version).2017; 11(6):521– 525.
- Kang DY. A brief discussion on the study of the real world.Chinese Journal of Cancer Prevention and treatment. 2017; 9(2):100–103.
- AIHW. Cervical screening in Australia 2012–2013. Cancer series no.93. Cat. no. CAN 91. Canberra: Australian Institute of Health and Welfare.2015.
- WHO. Comprehensive cervical cancer control-A guide to essential practice Second edition. Geneva: WHO Press.2014.
- Farhad A, Rainer K, & Belaynew W. Understanding cervical cancer in the context of developing countries. Annals of Tropical Medicine and Public Health.2012; 5(1), 3. https://doi.org/10.4103/1755-6783. 92871
- Murillo R, Almonte M, Pereira A, Ferrer E, Gamboa OA, Jero´nimo J,et al. Cervical Cancer Screening Programs in Latin America and the Caribbean. Vaccine.2008; 19; 26 Suppl 11:L37–48. https://doi.org/ 10.1016/j.vaccine.2008.06.013 PMID: 18945401
- Anttila A, von KL, Aasmaa A, Fender M, Patnick J, Rebolj M, et al. Cervical cancer screening policies and coverage in Europe. European Journal of Cancer. 2009; 45(15), 2649–2658. https://doi.org/10. 1016/j.ejca.2009.07.020 PMID: 19699081
- Arbyn M, Anttila A, Jordan J, Ronco G, Schenck U, Segnan N, et al. European Guidelines for Quality Assurance in Cervical Cancer Screening. Second edition—summary document. Annals of oncology: official journal of the European Society for Medical Oncology / ESMO. 2010; 21(3), 448–458. https://doi. org/10.1093/annonc/mdp471 PMID: 20176693
- Murillo R, Wiesner C, Cendales R, Piñeros M, Tovar S. Comprehensive evaluation of cervical cancer screening programs: the case of Colombia. Salud pu´blica de Me´xico,2011; 53(6), 469. PMID: 22282139
- MOH. Management Plan for Rural Areas Cervical Cancer and Breast Cancer Screening Examination Program. 2009 [cited 2009 June 24]; Available from: http://www.moh.gov.cn/fys/s7900/200906/ cd3c33a7ad624a50b8100b262041dabe.shtml.
- NHFPC. Notification about carry out major women and children’s public health program in 2013 [2013] No.65. ed. Maternal and Children’s Health Services.2013, Beijing.
- Abdul S, Brown BH, Milnes P, Tidy JA. The use of electrical impedance spectroscopy inthe detection of cervical intraepithelial neoplasia. Int J Gynecol Cancer 2006; 16, 1823–1832 https://doi.org/10.1111/j. 1525-1438.2006.00651.x PMID: 17009978
- Long SY, Lei W, Feng YK, Lv DH, Cai YX, Yang P. The feasibilities of TruScreen for primary cervical cancerscreening: a self-controlled study, Arch Gynecol Obstet. 2013; 288:113–118 https://doi.org/10. 1007/s00404-012-2697-4 PMID: 23296464
- Chen WQ, Sun KX, Zheng RS. Report of Cancer Incidence and Mortality in Different Areas of China, 2014.China Cancer.2018,;Vol. 27,N o.1
- WHO. Comprehensive cervical cancer control-A guide to essential practice Second edition. 2014, Geneva: WHO Press.
- Zhao QY, Dai Y, Dang L, Kong LH, Zhang Y, Feng RM, et al. Real-world research on cervical cancer screening program and effect evaluation for Chinese population. Chin J Oncol.2018; 40(10):764–771.
- Shi CX, Zhang ZH, and Zhao L, Analysis of the effect of Cervical Cancer examination Project and discussion on the Management Mode of positive cases in Jinchang City. Hospital management.2017; 20:420
